 Hasta cierto punto, las datos de PK/PD aplicados a las infecciones producidas por SARM con CMI elevadas a vancomicina han sido el punto de partida en el que muchos se han basado para afirmar que en estos pacientes la alternativa a vancomicina, habitualmente daptomicina, era de elección en el tratamiento de estas infecciones, aún en ausencia de datos clínicos que avalaran esta afirmación.
Hasta cierto punto, las datos de PK/PD aplicados a las infecciones producidas por SARM con CMI elevadas a vancomicina han sido el punto de partida en el que muchos se han basado para afirmar que en estos pacientes la alternativa a vancomicina, habitualmente daptomicina, era de elección en el tratamiento de estas infecciones, aún en ausencia de datos clínicos que avalaran esta afirmación.
En este artículo australiano de acceso libre (Holmes NE et al. Antibiotic Choice May Not Explain Poorer Outcomes in Patients With Staphylococcus aureus Bacteremia and High Vancomycin Minimum Inhibitory Concentrations. J Infect Dis. 2011;204(3):340–347) los autores se aproximan al problema del SARM con CMI elevada a vancomicina desde una óptica distinta: ¿es el antibiótico utilizado el responsable de los peores resultados clínicos observados? ¿hay otros factores dependientes del paciente o del microorganismo que lo justifican?
Se trata de un estudio observacional prospectivo multicéntrico en el que participaron 27 centros de Australia y Nueva Zelanda en los que se han recogido más de 7.000 bacteriemias por S. aureus. Sobre el total de bacteriemias se seleccionaron todos los casos de bactermia por SASM y SARM que entre enero de 2007 y noviembre de 2008 recibieron tratamiento con vancomicina. Cada paciente fue pareado con el siguiente paciente por orden de registro que había sido tratado con flucoxacilina. De todos estos pacientes se evaluaron: a) datos demográficos básicos (edad, sexo) b) el origen de la infección c) presencia de catéteres u otro material protésico d) presentación clínica e) sensibilidad o resistencia a meticilina f) tratamiento recibido y g) mortalidad a los 30 días. Desde el punto de vista metodológico la CMI a vancomicina se midió por E-Test y por dilución en caldo.
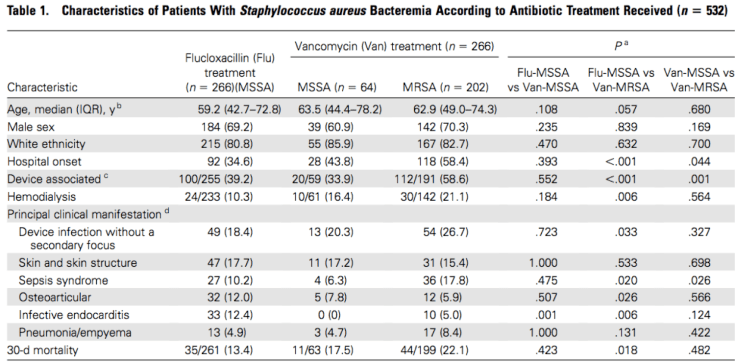
Se incluyeron 568 pacientes con bacteriemia por S. aureus (60% SASM), 284 de los cuales habían recibido vancomicina. Las características de los pacientes aparecen en la Tabla 1:
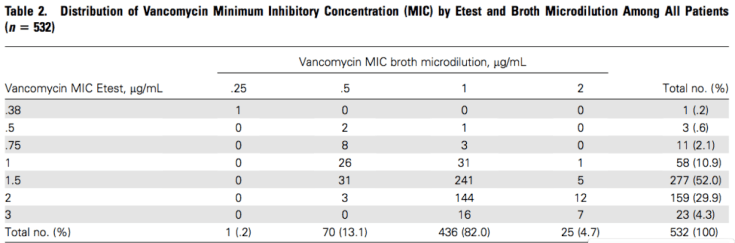
La distribución de CMI a vancomicina en SASM y SARM, tanto por CMI como por microdilución, se expresan en la Tabla 2. Tan sólo el 0.4% de los aislamientos fueron de hVISA. Respecto a la CIM de vancomicina en SASM, el 26% de los casos tuvieron una CMI por E-test >1.5 mcg/ml.
En cuanto a la relación entre mortalidad y CMI a vancomicina se observó que ésta era mayor conforme se incrementaba la CMI, tanto por E-test como por microdilución. Este incremento de mortalidad en pacientes con bacteriemias por S. aureus cuyas CMI estaban por encima de 1.5 mcg/ml (E-test) [12.2% vs 26.8%; OR 2.64 (IC95 1.66-4.17)] se observó tanto en pacientes con infecciones por SARM tratados con vancomicina como en pacientes con infecciones por SASM tratados con flucoxacilina (Gráfica 1).
En el análisis multivariante en el que se incluyeron todos los determinantes a priori potencialmente relacionados con mortalidad, los únicos factores que resultaron independientemente relacionados con la mortalidad fueron: a) origen hospitalario de la infección b) edad y c) CMI >1.5 mcg/ml. Sin embargo la meticilín resistencia (SASM vs SARM) no resultó significativo. A diferencia del estudio de Soriano del CID en este estudio la probabilidad de presentación con sepsis fue mayor con CMI >1.5 mcg/mL.
Este estudio demuestra por primera vez que debe haber otros factores distintos a la eficacia de la vancomicina implicada en un peor pronóstico de estos pacientes con infecciones por S. aureus con CIM a vancomicina >1.5 mcg/mL. Esto implica que es posible que la utilización de un agente alternativo a la vancomicina no mejore el pronóstico de estos pacientes.
Los autores plantean que una CMI >1.5 mcg/mL en S. aureus puede ser un marcador de fragilidad del paciente (edad, nosocomialidad, etc) o de mayor agresividad del microorganismo.


Deja un comentario